Nach Implantation von Gewebeersatzmaterialien erfahren Patienten oft langwierige Behandlungen. Einer der Gründe ist das Fehlen geeigneter Werkzeuge, um den Regenerationsprozess überwachen zu können, der stark von der lokalen Sauerstoffversorgung des Implantatmilieus abhängt.
Ziel des Projektvorhabens war die Entwicklung eines implantierbaren fluoreszenz-optischen Sauerstoff-Mikrosensors mit mobilem und autonom arbeitendem Datenlogger zur Bestimmung des lokalen Sauerstoffgehalts in Mikroumgebungen („Hot Spots“) für in vitro und in vivo Anwendungen in der regenerativen Medizin.

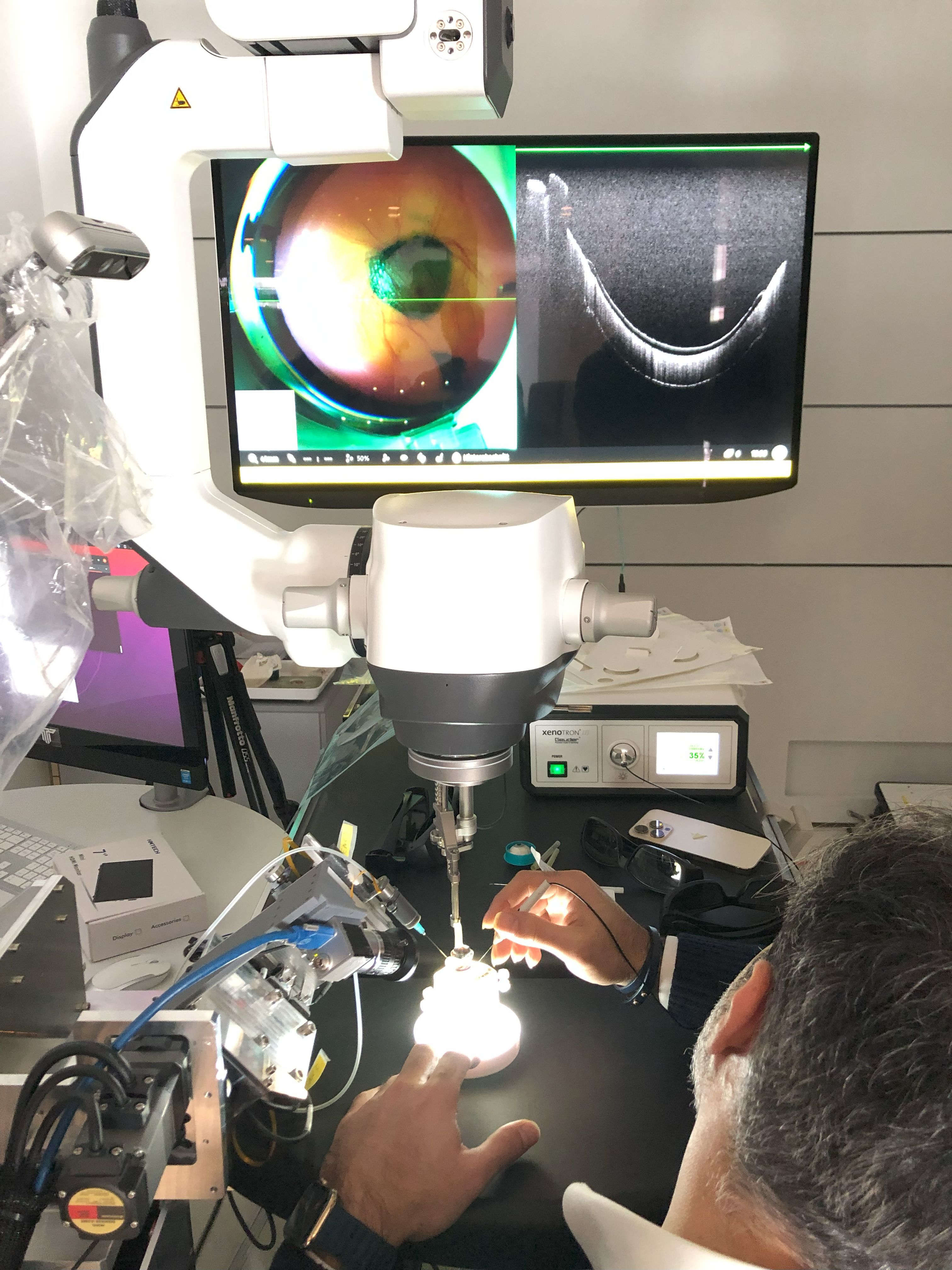
Im Projekt wurden erfolgreich verschiedene sensorische Anwendungskonzepte zu einer mächtigen neuen sensorischen Toolbox kombiniert, die im gesamten Anwendungsbereich von in vitro über ex vivo bis hin zu in vivo eingesetzt werden kann. Diese Multifunktionalität basiert auf der Verwendung von jeweils gleichem Sensormaterial (kein Technologiebruch), das sowohl als Mikrosensor mit örtlicher Auflösung von 40 µm, als auch als Millimeter-Sonde und als großflächiger Sensor für Imaging-Anwendungen bereitgestellt werden kann. Der im Projekt als zentrales Ziel entwickelte in vivo Logger wurde realisiert und steht für weitere Verwendungen bereit. Er kann als Komplettimplantat in größeren Tieren verwendet werden, bei Nagern wird der Mikrosensor-Lichtleiter implantiert und der Logger als „Rucksack“ platziert.
Weitere wichtige Ergebnisse sind neue Mikrotiterplatten-Inserts, die in vitro die Erfassung von O2-Gradienten in vielen Wells gleichzeitig ohne mechanische Hilfe und kabelloses Auslesen via Imaging Systeme erlauben. Darüber hinaus wurde eine innovative Integration von Mikrosensoren in eine motorisierte Plattform zum automatisierten Auffinden und Beschreiben von Oxygenierungszuständen in der 3D Zellzucht realisiert.